Was ist Stammzellsekretom? Was sind Exosomen?
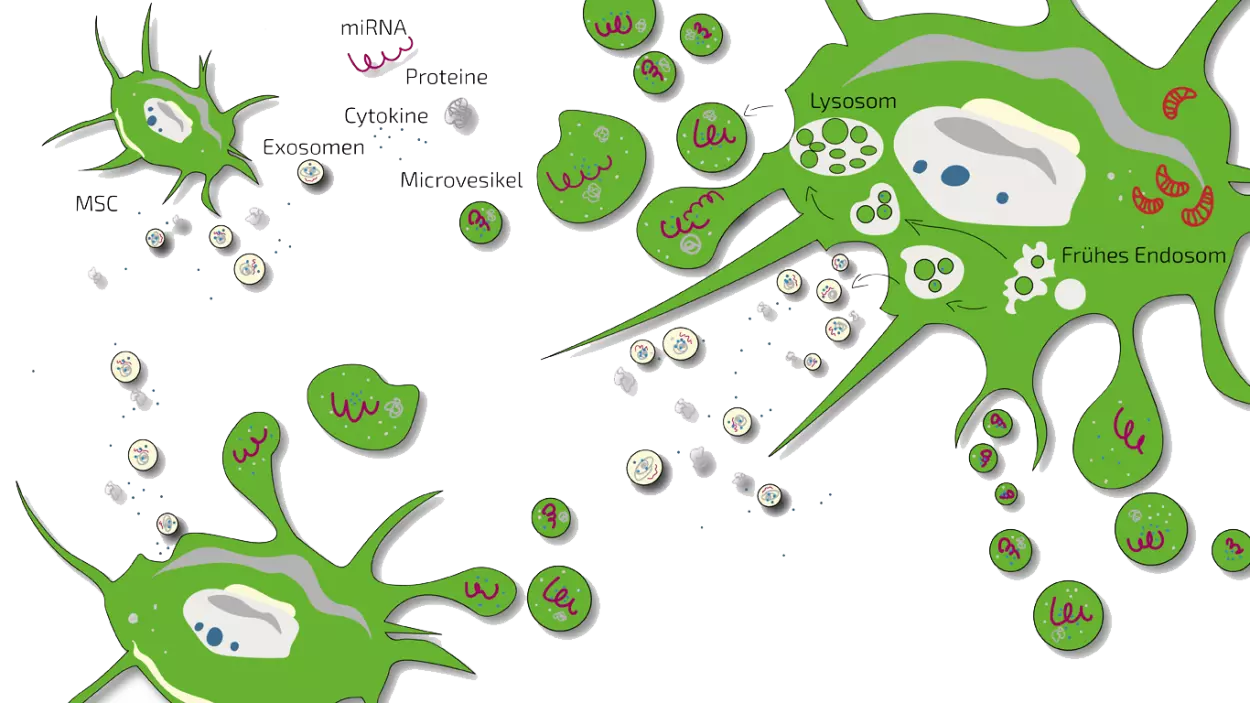
Als Sekretom von Stammzellen bezeichnet man wissenschaftlich die Gesamtheit aller von Stammzellen nach außen abgegebenen Stoffe . Diese beinhalten u.a. Mikrovesikel, Exosomen, Proteine (Eiweiße), Cytokine (Zell-Botenstoffe), Hormon-ähnliche Stoffe und andere sogenannte immunmodulierende Stoffe.
Auf Grundlage der aktuellen Wissenschaft geht man davon aus, dass die Wirkung von Stammzellen in bisher durchgeführten klinischen Studien nicht von den Zellen als solches ausgeht, sondern über die von den Zellen abgegebenen Vesikel, Eiweißmoleküle und weitere Stoffe wie Cytokine. Diese nach außen abgegebenen Stoffe nennt man als Überbegriff „das Sekretom“, weil die Abgabe als Sekretion bezeichnet wird. Welche Stoffe des Sekretoms die eigentlichen Wirkungen auslösen ist bisher weitestgehend unbekannt. Das ANOVA IRM Sekretom wird aus autologen, mesenchymalen Stammzellen hergestellt.
Springen Sie direkt zu folgenden Themen:
- Vergleich Sekretom und Exosomen
- Vorteile einer Sekretom-Therapie
- Ablauf einer Sekretom-Behandlung
- Häufig gestellte Fragen
- Quellen und Literatur
Folgende Erkrankungen behandeln wir mit Sekretom:
- Poly-Arthritis
- Poly-Arthrose
- Chronisch entzündliche Erkrankungen
- Risse und Anrisse von Bändern, Ligamenten an der Wirbelsäule
- Verletzungen der Wirbelsäule, Verletzungen des Rückenmarks
- Rückenmarksdurchtrennungen (teilweise Durchtrennungen und in Kombination mit anderen Therapien auch vollständige Durchtrennungen)
- Chronische Schmerzen und Entzündungen an der Wirbelsäule
- Erektile Dysfunktion, Impotenz
Ist das Sekretom das gleiche wie Exosomen?
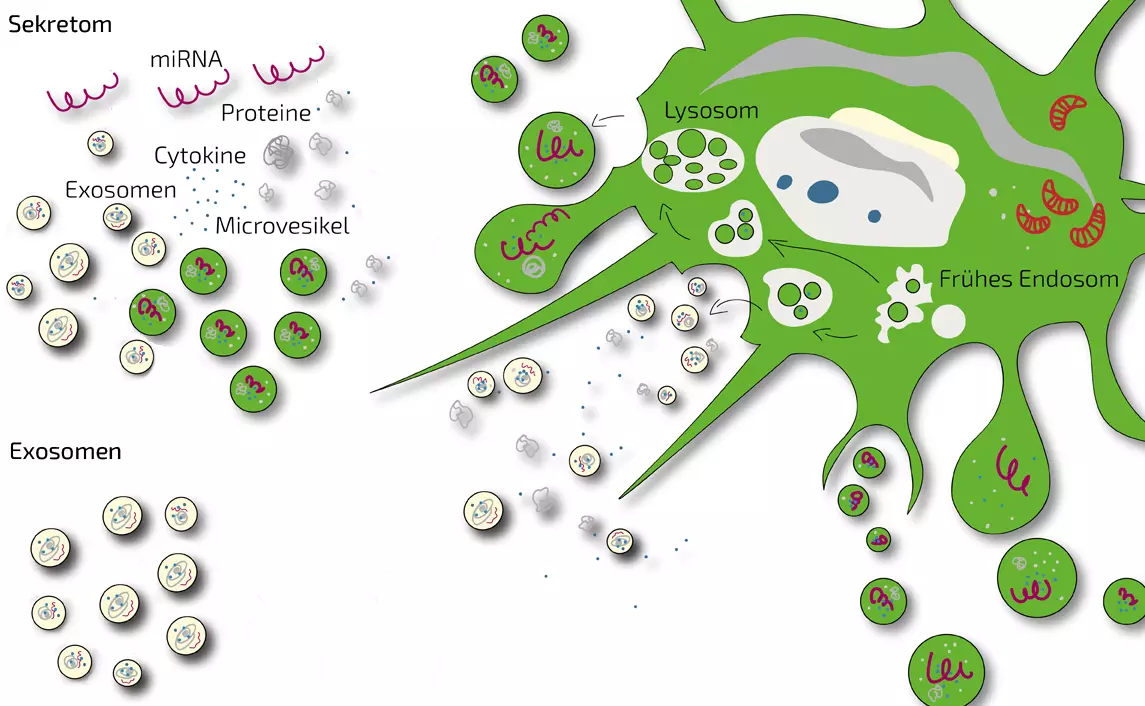
Sekretom und Exosomen werden manchmal wie Synonyme benutzt, sind jedoch eigentlich unterschiedlich zu werten.
Das Sekretom ist die Gesamtheit aller nach außen abgegebenen Botenstoffe einschließlich der Mikrovesikel und Exosomen, aber darüber hinaus noch weitere wichtige Faktoren, die gelöst in der Flüssigkeit vorliegen. Hierzu gehören viele regenerationsfördernde Wachstumsfaktoren und sogenannte Cytokine (Zell-Zell-Botenstoffe).
Exosomen dagegen sind eigentlich nur die partikulären Exosomen, die aus der Gesamtheit isoliert werden. Durch die Isolation werden sie aufkonzentriert, jedoch gehen die wichtigen gelösten Stoffe und Microvesikel verloren.
Was ist eine Stammzellsekretom Therapie?
Die Stammzellsekretom-Therapie der ANOVA IRM ist eine experimentelle Therapie, die wir im Rahmen einer individuellen Behandlung bei Patienten anwenden, die einen eindeutigen Nutzen von der Therapie haben könnten. Bei der Stammzellsekretom-Therapie werden aus dem eigenen Fett-Gewebe des Patienten Stammzellen gewonnen (autologe Stammzellen, Fettstammzellen, adipogene Stammzellen, ADSCs). Diese initial geringe Anzahl an Stammzellen wird im Labor gezüchtet und expandiert (vermehrt). Hierdurch kann man deutlich mehr Stammzellen gewinnen als bei einer Therapie mit BMC, bei der das gewonnene Knochenmark konzentriert wird, aber keine Vermehrung der darin vorliegenden Stammzellen erfolgt. Ziel dieses Prozesses ist es, die Anzahl an Stammzellen zu erhöhen, die Produktion der potentiell regenerativen und entzündungshemmenden Substanzen, die Stammzellen nach außen abgeben, zu induzieren, zu konzentrieren und für die Behandlung einzusetzen. Anstatt dem Patienten Stammzellen zu implantieren oder zu injizieren, werden nur die produzierten extrazellulären, nach außen abgegebenen Komponenten, also das Sekretom, appliziert. Im Vergleich zur direkten Injektion von Stammzellen sind die Risiken dieser Methode relativ gesehen geringer.
Was sind die Vorteile einer Behandlung mit
Stammzellsekretom gegenüber Stammzellen
Kurz zusammengefasst kann man sagen, dass im Vergleich zum BMC reine Stammzellen gewonnen werden und mehrere Dosen aus einer Gewebeentnahme gewonnen werden können, weswegen es sich besonders für die Behandlung chronischer Erkrankungen eignet. Darüber hinaus ist das Sekretom lagerbar, vor der Anwendung voll qualitätskontrolliert und wird von 90-98% reinen MSC (mesenchymalen Stammzellen) hergestellt.
Die Verwendung von Stammzellen ist in den meisten Ländern immer noch limitiert. Dies hat ihre Verwendung in der Medizin trotz ihrer vermuteten und teilweise klinisch belegten Wirksamkeit bei der Behandlung vieler chronischer oder unheilbarer Krankheiten stark eingeschränkt. Grund hierfür sind unter anderem, dass Stammzellen bei zu starker Expansion ihre Wirksamkeit einbüßen können, veränderte Zellen wie z.B. Krebszellen entstehen können und dass Stammzellen, zumindest diejenigen, die aus Blut stammen (hämatopoietische Stammzellen), beim Einfrieren verändert werden, was wiederum die potentielle Wirksamkeit, also auch die Zusammensetzung der nach außen abgegebenen Stoffe verändert.
Dies könnte sich jetzt ändern, mit einem der neuesten Durchbrüche in der Stammzellforschung: Das ANOVA IRM Wissenschaftsteam hat einen Prozess entwickelt und implementiert, der die evidenzbasiert als therapeutisch aktiv eingestuften Komponenten von Stammzellen gewinnt und konzentriert - das Stammzellsekretom.
Das Sekretom der ANOVA IRM wird aus mild expandierten (also potentiell weniger veränderten Zellen) hergestellt. Die Zusammensetzung ist somit die unter den speziellen Kulturbedingungen natürliche, die nicht durch verlängerte Kultur oder Einfrieren verändert wird. Dies bedeutet, dass das Sekretom aus weniger Zellen, aber potentiell hochwertigeren Zellen hergestellt wird.
Nach der Produktion kann das Sekretom in dieser Zusammensetzung gelagert werden. Exosomen und andere im Sekretom enthaltene Stoffe bleiben stabil. Dies erlaubt mit einer Entnahme zahlreiche Dosen herzustellen, die dann über 2 Jahre genutzt werden können. Somit ist die Behandlung mit Sekretom vor allem für chronische Krankheiten die bessere Option.
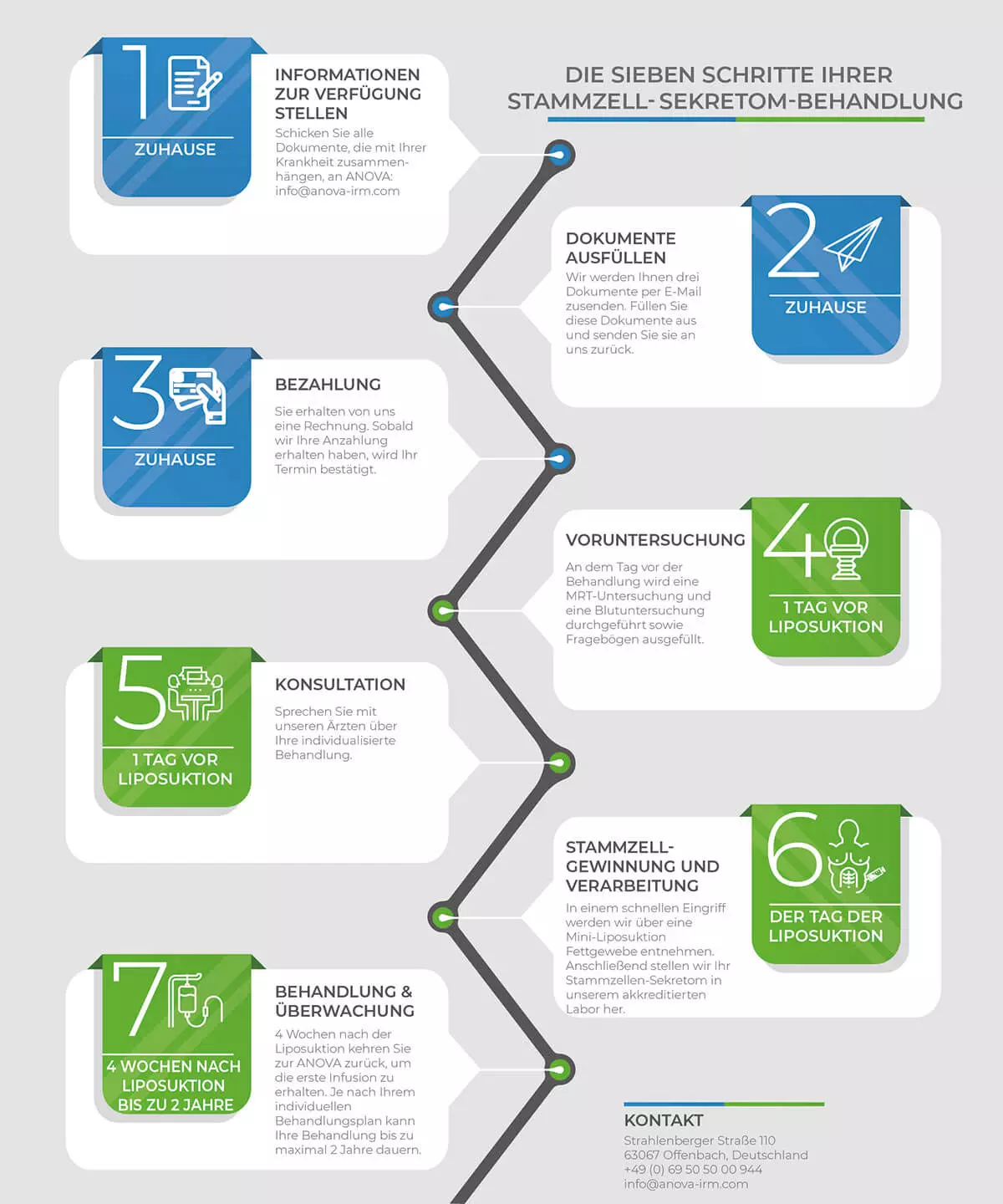
Ablauf einer Gewinnung von Sekretom für die Stammzell-Therapie
Nachfolgend ist der Ablauf einer Gewinnung von Sekretom in 3 Schritten dargestellt. Die anschließende Therapie kann sich über wenige Wochen bis 2 Jahre erstrecken.
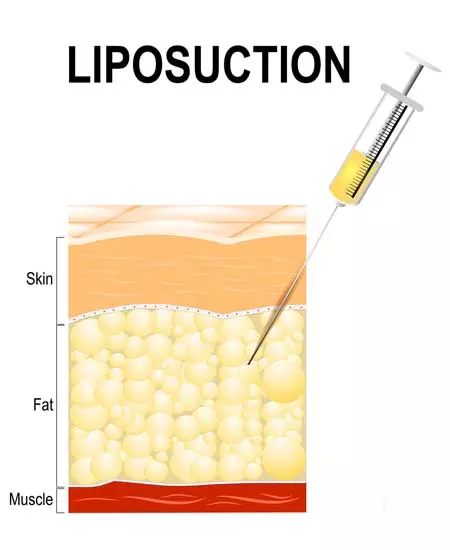
Liposuction
Schritt 1 - Gewinnung von mesenchymalen Stammzellen (MSCs) aus subkutanem Fettgewebe
In der ANOVA verwenden wir die sogenannte "Nutational Infrasonic Liposuction", bei der das Euromi Lipomatic®-System zum Einsatz kommt. Dieses Verfahren liefert 10- bis 100-mal mehr lebensfähige MSCs, die aus dem gewonnenen Fettgewebe isoliert werden, als jede andere Technik.
Das Fettgewebe wird sofort in einem behördlich-kontrollierten, GMP-zertifizierten Reinraum (Klasse A) verarbeitet, um die höchstmögliche Qualität und Sicherheit des Endprodukts zu gewährleisten.
Schritt 2 - Verarbeitung der Stammzellen und Produktion des Stammzellsekretoms (SCS)
In unseren spezialisierten Labors wird die „Stromal Vascular Fraction“ (SVF) nach enzymatischer Verdauung aus Fettgewebe isoliert. Die SVF ist eine Mischung verschiedener Zelltypen. Es enthält einen niedrigen Prozentsatz an MSCs (entspricht bis zu 500.000 Zellen pro Gramm), obwohl dies eine der höchsten Konzentrationen an MSCs im menschlichen Körper ist.
Im nächsten Schritt werden die MSCs kultiviert und vermehrt, bis sie die gewünschte Menge erreicht haben. Hierbei erhöht sich die Reinheit auf 90-98%. Indem die Zellen externen Stimuli ausgesetzt werden, werden sie dazu angeregt, eine hohe Konzentration von Cytokine, miRNAs und Wachstumsfaktoren (die die Regenerationsfähigkeit beibehalten) abzuscheiden, die in extrazellulären Vesikeln (Mikrovesikeln und Exosomen) verpackt sind. Zusammen bilden diese Faktoren das Sekretom.
Nach einer umfassenden Qualitätskontrolle ist das Stammzellsekretom gebrauchsfertig und kann mehrere Monate bei minus 80°C gelagert werden. Dies ermöglicht die Erstellung eines Therapieplans, der mehrere Infusionen (über 2 Jahre) und optimale Behandlungsergebnisse ermöglicht.

Vermehrung der MSC

Anwendung
Schritt 3 - Anwendung und Behandlung mit der Stammzellsekretomtherapie von ANOVA IRM
Aus einer einzelnen Isolation von Stammzellen, aus der Absaugung des Fettgewebes, können 10 therapeutische Dosen erhalten werden, die systemisch (intravenös) über eine Infusion verabreicht werden sollen. Die früheste Anwendung des Stammzellsekretoms ist 4 Wochen nach der Fettabsaugung möglich. Während dieser Zeit bereiten unsere Biologen im Labor das Produkt vor und konzentrieren es. Parallel dazu werden mehrere Qualitätstests auf pharmazeutischer Ebene durchgeführt, um sicherzustellen, dass das Produkt sicher ist und den höchsten Qualitätsstandards entspricht, die wir anstreben.
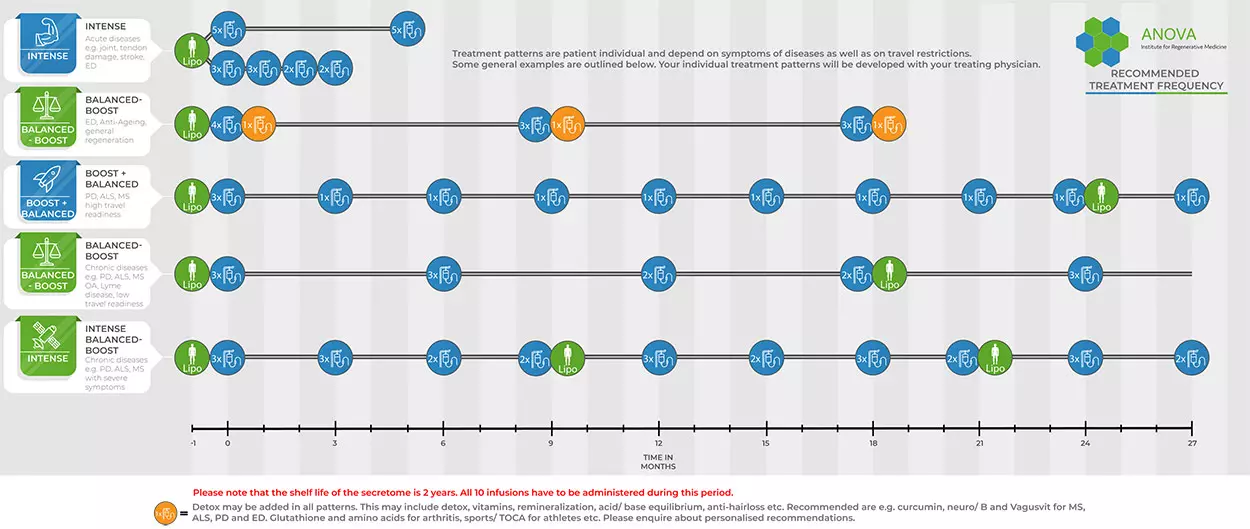
Individuelle Behandlungspläne - Injektion
Bei der Erstellung Ihres Behandlungsplans werden sowohl die krankheitsspezifischen Faktoren als auch Ihre spezielle Situation als PatientIn mit einbezogen. Generell stehen nach der Liposuktion 10 Dosen zur Verfügung. Je nach Krankheit und Stadium erfolgen die Behandlungen bei akuten Erkrankungen eher in kurzer Folge aufeinander (intense, Abbildung unten), bei chronischen Erkrankungen in regelmäßigen Abständen. Für PatientInnen aus Deutschland und umliegenden Ländern wie Österreich, der Schweiz, Italien, den Niederlanden, Großbritannien, Frankreich, Spanien etc. ist eine Anreise meist einfach und wenig kostenintensiv mehrfach zu realisieren. Daher werden die Injektionen meist einmalig als Mehrfach-Dosis und nachfolgend als einzelne Injektionen in 6-8 Wochen Abstand geplant (boost+balanced). Bei PatientInnen aus den weit entfernten Regionen wie den USA, Kanada, Südamerika, Brasilien, dem Nahen Osten, Saudi Arabien, Oman, Russland etc. dagegen werden die Behandlungen meist kontinuierlich als Mehrfach-Dosis aber in größerem Abstand geplant, um die Anzahl der Anreisen zu reduzieren.
Kontraindikationen
Unsere Stammzellbehandlungen sind experimentell, aber wir behandeln nur solche Patienten, von denen wir auf Grundlage des Standes der Medizin, also der medizinisch-wissenschaftlichen Evidenz davon ausgehen, dass das Risiko/Nutzen-Verhältnis eine Behandlung indiziert.
Bitte haben Sie Verständnis dafür, dass wir daher keine Patienten behandeln auf die folgende Punkte zutreffen:
- Aktive Krebserkrankung in den letzten zwei Jahren
- Noch nicht volljährig
- Bestehende Schwangerschaft oder Stillzeit
- Nicht in der Lage, selbständig zu atmen, bzw. Verwendung eines Beatmungsgeräts
- Schwierigkeiten mit der Atmung in Rückenlage
- Dysphagie (extreme Schluckbeschwerden)
- Psychiatrische Erkrankung
- Aktive Infektionskrankheit (Hepatitis A, B, C, HIV, Syphilis etc.)
Häufig gestellte Fragen - FAQ - Sekretom - Exosomen
Weitere Informationen finden Sie auch in unserem allgemeinen Blog-Post: Das Potential von Exosomen erklärt.
Vokabeln und Definitionen
Differenzierung - Stammzellen haben das Potential sich je nach äußeren Stimuli und Signalen in verschiedene Zelltypen zu entwickeln = differenzieren. MSC z.B. müssen mind. Knochenzellen, Knorpelzellen und Fettzellen werden können, um als Stammzelle bezeichnet werden zu dürfen.
Krebs, Krebszelle - Zellen, bei denen die normale Regulierung der Zellteilung nicht mehr funktional ist. Diese Zellen teilen sich, obwohl dies nicht notwendig wäre und vermehren sich so zum Schaden des Organismus immer weiter.
Morphologie - Die Gestalt, das Aussehen der Zellen im Mikroskop
Proliferation - Zellteilung, Zellvermehrung
Stammzelle - eine Zelle, die in ihrer Vermehrung ein größeres Potential hat als normale Körperzellen. Sie kann sich selbst erneuern und in mehrere Zelltypen differenzieren = funktionalisieren.
Was ist das Sekretom?
Stammzellen kommunizieren mir anderen Zellen indem sie Botenstoffe nach außen abgeben. Die Gesamtheit aller abgegebenen Stoffe wird als Sekretom (von Sekretion = Abgabe nach außen) bezeichnet. Das Sekretom kann Exosome, Microvesikel, Proteine, Wachstumsfaktoren, Hormone, Cytokine und weitere Stoffe enthalten. Einen wissenschaftlichen Übersichtsartikel zu Vesikeln finden Sie hier.
Was sind Exosomen?
Exosomen sind kleine Botenpakete, die Zellen nach außen abgeben. Exosomen sind ca. 30-100nm (also 0,00003 bis 0,0001mm) groß und bestehen aus einer äußeren Doppel-Lipid-Schicht (wie Liposomen) und einem Innenraum, der mit Flüssigkeit und Botenstoffen wie miRNA und Proteinen beladen sein kann. Exosomen werden durch die Fusion von multi-vesikulären Körperchen im Zellinneren mit der Zellmembran nach außen abgegeben. Dort können sie von anderen Zellen aufgenommen werden und so Reaktionen vermitteln. Einen wissenschaftlichen Übersichtsartikel zu Vesikeln finden Sie hier.
Was sind Mikrovesikel?
Mikrovesikel sind ebenfalls Lipid-Membran-umhüllte Partikel, die Ladung tragen können. Jedoch sind sie mit 100 bis 1.000nm größer als Exosomen und werden durch Abschnürung an der Zellmembran nach außen abgegeben. Einen wissenschaftlichen Übersichtsartikel zu Vesikeln finden Sie hier.
Was sind Wachstumsfaktoren?
Zellen reagieren auf ihre Umgebung. Sie teilen sich nur dann, wenn dies notwendig ist. Im gesunden Körper teilt sich eine Leberzelle z.B. nur einmal im Jahr, um abgestorbene Zellen zu ersetzen. Das Signal, dass eine Zelle sich teilen soll, kann der Verlust von Nachbarzellen sein (Schnittwunde) oder von anderen Zellen gebildete Wachstumsfaktoren. Diese Faktoren diffundieren zu anderen Zellen, binden an Rezeptoren auf der Oberfläche und lösen im Inneren der Zielzelle Signalkaskaden aus, die die Teilung anregen. Durch Entzündungen wird oft die Zellteilung (Proliferation) gehemmt.
Woraus wird das Sekretom hergestellt?
Das Sekretom, dass das ANOVA Institut für regenerative Medizin anwendet, wird aus mesenchymalen Stammzellen des Patienten hergestellt. Diese werden in einer kurzen Mini-Liposuktion aus dem Bauch-Fett gewonnen und nachfolgend sehr schonend kultiviert und so vermehrt (s.u.). Das Ausgangsmaterial ist nach der Fettgewinnung das hieraus isolierte SVF (stromal vascular fraction), das nur ca. 1-10% MSCs und Vorläuferzellen enthält. Nachfolgend werden die MSCs kultiviert, vermehrt und hierdurch eine zu 90-98% aus MSCs bestehende Reinkultur gewonnen. Das diese Zellen teilungsaktive Stammzellen sind, haben wir mit einem sogenannten Multi-Differenzierungsnachweis nachgewiesen. In diesem lässt man die MSC über 2-3 Wochen in Zellarten (Knorpelzellen, Knochenzellen und Fettzellen) differenzieren. Wenn dies gelingt, hat man einen von mehreren Beweisen, dass es sich tatsächlich um Stammzellen handelt. Zusätzlich kontrollieren wir jede Charge auf Reinheit.
Mehr Stammzellen - bessere Wirkung?
Viele PatientInnen glauben, dass eine größere Menge an Stammzellen auch bessere Effekte erzielt. Dies ist bis zu einer schwer definierbaren Grenze auch richtig. Da man die "Wirksamkeit" jedoch bisher nicht oder nur in sehr wenigen Fällen messen kann, sollte man hier sehr vorsichtig sein. Viele Charakteristika von Stammzellen sind bisher nicht gut verstanden und niemand weiß, welche Faktoren und Stoffe genau eine Wirkung definieren. Das Einzige was man wirklich genau weiß, ist, dass mit zunehmender Vermehrung (Generationen, Populationsverdopplungen und Passagen) das Wirkpotential nachlässt. Das heißt je mehr man Stammzellen vermehrt, umso weniger ist es wahrscheinlich, dass sie noch wirksam sind.
Viele PatientInnen glauben, dass eine größere Menge an Stammzellen auch bessere Effekte erzielt. Dies ist bis zu einer schwer definierbaren Grenze auch richtig. Da man die "Wirksamkeit" jedoch bisher nicht oder nur in sehr wenigen Fällen messen kann, sollte man hier sehr vorsichtig sein. Viele Charakteristika von Stammzellen sind bisher nicht gut verstanden und niemand weiß, welche Faktoren und Stoffe genau eine Wirkung definieren. Das Einzige was man wirklich genau weiß, ist, dass mit zunehmender Vermehrung (Generationen, Populationsverdopplungen und Passagen) das Wirkpotential nachlässt. Das heißt je mehr man Stammzellen vermehrt, umso weniger ist es wahrscheinlich, dass sie noch wirksam sind.
Was sind die Vorteile des Sekretoms?
Viele PatientInnen glauben, dass eine größere Menge an Stammzellen auch bessere Effekte erzielt. Dies ist bis zu einer schwer definierbaren Grenze auch richtig. Da man die "Wirksamkeit" jedoch bisher nicht oder nur in sehr wenigen Fällen messen kann, sollte man hier sehr vorsichtig sein. Viele Charakteristika von Stammzellen sind bisher nicht gut verstanden und niemand weiß, welche Faktoren und Stoffe genau eine Wirkung definieren. Das Einzige was man wirklich genau weiß, ist, dass mit zunehmender Vermehrung (Generationen, Populationsverdopplungen und Passagen) das Wirkpotential nachlässt. Das heißt je mehr man Stammzellen vermehrt, umso weniger ist es wahrscheinlich, dass sie noch wirksam sind.
Viele PatientInnen glauben, dass eine größere Menge an Stammzellen auch bessere Effekte erzielt. Dies ist bis zu einer schwer definierbaren Grenze auch richtig. Da man die "Wirksamkeit" jedoch bisher nicht oder nur in sehr wenigen Fällen messen kann, sollte man hier sehr vorsichtig sein. Viele Charakteristika von Stammzellen sind bisher nicht gut verstanden und niemand weiß, welche Faktoren und Stoffe genau eine Wirkung definieren. Das Einzige was man wirklich genau weiß, ist, dass mit zunehmender Vermehrung (Generationen, Populationsverdopplungen und Passagen) das Wirkpotential nachlässt. Das heißt je mehr man Stammzellen vermehrt, umso weniger ist es wahrscheinlich, dass sie noch wirksam sind.
Weiterführende Literatur zu MSC, BMC, Stamzellen Secretom und EVs
- Georg Hansmann, Philippe Chouvarine, Franziska Diekmann, Martin Giera, Markus Ralser, Michael Mülleder, Constantin von Kaisenberg, Harald Bertram, Ekaterina Legchenko & Ralf Hass "Human umbilical cord mesenchymal stem cell-derived treatment of severe pulmonary arterial hypertension". Nature Cardiovascular Research volume 1, pages568–576 (2022).
- Murphy JM, Fink DJ, Hunziker EB, et al. Stem cell therapy in a caprine model of osteoarthritis . Arthritis Rheum. 2003;48:3464–74.
- Lee KB, Hui JH, Song IC, Ardany L, et al. Injectable mesenchymal stem cell therapy for large cartilage defects—a porcine model. Stem Cell. 2007;25:2964–71.
- Saw KY, Hussin P, Loke SC, et al. Articular cartilage regeneration with autologous marrow aspirate and hyaluronic acid: an experimental study in a goat model. Arthroscopy . 2009;25(12):1391–400.
- Black L, Gaynor J, Adams C, et al. Effect of intra-articular injection of autologous adipose-derived mesenchymal stem and regenerative cells on clinical signs of chronic osteoarthritis of the elbow joint in dogs. Vet Ther. 2008;9:192-200.
- Centeno C, Busse D, Kisiday J, et al. Increased knee cartilage volume in degenerative joint disease using percutaneously implanted, autologous mesenchymal stem cells. Pain Physician. 2008;11(3):343–53.
- Centeno C, Kisiday J, Freeman M, et al. Partial regeneration of the human hip via autologous bone marrow nucleated cell transfer: a case study. Pain Physician. 2006;9:253–6.
- Centeno C, Schultz J, Cheever M. Safety and complications reporting on the re-implantation of culture-expanded mesenchymal stem cells using autologous platelet lysate technique. Curr Stem Cell. 2011;5(1):81–93.
- Pak J. Regeneration of human bones in hip osteonecrosis and human cartilage in knee osteoarthritis with autologous adipose derived stem cells: a case series. J Med Case Rep. 2001;5:296.
- Kuroda R, Ishida K, et al. Treatment of a full-thickness articular cartilage defect in the femoral condyle of an athlete with autologous bone-marrow stromal cells. Osteoarthritis Cartilage. 2007;15:226–31.
- Emadedin M, Aghdami N, Taghiyar L, et al. Intra-articular injection of autologous mesenchymal stem cells in six patients with knee osteoarthritis. Arch Iran Med. 2012;15(7):422–8.
- Saw KY et al. Articular cartilage regeneration with autologous peripheral blood stem cells versus hyaluronic acid: a randomized controlled trial. Arthroscopy. 2013;29(4):684–94.
- Vangsness CT, Farr J, Boyd J, et al. Adult human mesenchymal stem cells delivered via intra-articular injection to the knee following partial medial meniscectomy. J Bone Joint Surg. 2014;96(2):90–8.
- Freitag, Julien, et al. Mesenchymal stem cell therapy in the treatment of osteoarthritis: reparative pathways, safety and efficacy–a review. BMC musculoskeletal disorders 17.1 (2016): 230.
- Maumus, Marie, Christian Jorgensen, and Danièle Noël. " Mesenchymal stem cells in regenerative medicine applied to rheumatic diseases: role of secretome and exosomes. " Biochimie 95.12 (2013): 2229-2234.
- Dostert, Gabriel, et al. " How do mesenchymal stem cells influence or are influenced by microenvironment through extracellular vesicles communication?. " Frontiers in Cell and Developmental Biology 5 (2017).
- Chaparro, Orlando, and Itali Linero. " Regenerative Medicine: A New Paradigm in Bone Regeneration. " (2016).
- Toh, Wei Seong, et al. " MSC exosome as a cell-free MSC therapy for cartilage regeneration: Implications for osteoarthritis treatment. " Seminars in Cell & Developmental Biology. Academic Press, 2016.
- Chaparro, Orlando, and Itali Linero. " Regenerative Medicine: A New Paradigm in Bone Regeneration. " (2016).
- S. Koelling, J. Kruegel, M. Irmer, J.R. Path, B. Sadowski, X. Miro, et al., Migratory chondrogenic progenitor cells from repair tissue during the later stages of human osteoarthritis , Cell Stem Cell 4 (2009) 324–335.
- B.A. Jones, M. Pei, Synovium-Derived stem cells: a tissue-Specific stem cell for cartilage engineering and regeneration , Tissue Eng. B: Rev. 18 (2012) 301–311.
- W. Ando, J.J. Kutcher, R. Krawetz, A. Sen, N. Nakamura, C.B. Frank, et al., Clonal analysis of synovial fluid stem cells to characterize and identify stable mesenchymal stromal cell/mesenchymal progenitor cell phenotypes in a porcine model: a cell source with enhanced commitment to the chondrogenic lineage, Cytotherapy 16 (2014) 776–788.
- K.B.L. Lee, J.H.P. Hui, I.C. Song, L. Ardany, E.H. Lee, Injectable mesenchymal stem cell therapy for large cartilage defects—a porcine model, Stem Cells 25 (2007) 2964–2971.
- W.-L. Fu, C.-Y. Zhou, J.-K. Yu, A new source of mesenchymal stem cells for articular cartilage repair: mSCs derived from mobilized peripheral blood share similar biological characteristics in vitro and chondrogenesis in vivo as MSCs from bone marrow in a rabbit model , Am. J. Sports Med. 42 (2014) 592–601.
- X. Xie, Y. Wang, C. Zhao, S. Guo, S. Liu, W. Jia, et al., Comparative evaluation of MSCs from bone marrow and adipose tissue seeded in PRP-derived scaffold for cartilage regeneration , Biomaterials 33 (2012) 7008–7018.
- E.-R. Chiang, H.-L. Ma, J.-P. Wang, C.-L. Liu, T.-H. Chen, S.-C. Hung, Allogeneic mesenchymal stem cells in combination with hyaluronic acid for the treatment of osteoarthritis in rabbits , PLoS One 11 (2016) e0149835.
- H. Nejadnik, J.H. Hui, E.P. Feng Choong, B.-C. Tai, E.H. Lee, Autologous bone marrow–derived mesenchymal stem cells versus autologous chondrocyte implantation: an observational cohort study , Am. J. Sports Med. 38 (2010) 1110–1116.
- I. Sekiya, T. Muneta, M. Horie, H. Koga, Arthroscopic transplantation of synovial stem cells improves clinical outcomes in knees with cartilage defects , Clin. Orthop. Rel. Res. 473 (2015) 2316–2326.
- Y.S. Kim, Y.J. Choi, Y.G. Koh, Mesenchymal stem cell implantation in knee osteoarthritis: an assessment of the factors influencing clinical outcomes , Am. J. Sports Med. 43 (2015) 2293–2301.
- W.-L. Fu, Y.-F. Ao, X.-Y. Ke, Z.-Z. Zheng, X. Gong, D. Jiang, et al., Repair of large full-thickness cartilage defect by activating endogenous peripheral blood stem cells and autologous periosteum flap transplantation combined with patellofemoral realignment , Knee 21 (2014) 609–612.
- Y.-G. Koh, O.-R. Kwon, Y.-S. Kim, Y.-J. Choi, D.-H. Tak, Adipose-derived mesenchymal stem cells with microfracture versus microfracture alone: 2-year follow-up of a prospective randomized trial , Arthrosc. J. Arthrosc. Relat. Surg. 32 (2016) 97–109.
- T.S. de Windt, L.A. Vonk, I.C.M. Slaper-Cortenbach, M.P.H. van den Broek, R. Nizak, M.H.P. van Rijen, et al., Allogeneic mesenchymal stem cells stimulate cartilage regeneration and are safe for single-Stage cartilage repair in humans upon mixture with recycled autologous chondrons , Stem Cells (2016) (n/a-n/a).
- L. da Silva Meirelles, A.M. Fontes, D.T. Covas, A.I. Caplan, Mechanisms involved in the therapeutic properties of mesenchymal stem cells , Cytokine Growth Factor Rev. 20 (2009) 419–427.
- W.S. Toh, C.B. Foldager, M. Pei, J.H.P. Hui, Advances in mesenchymal stem cell-based strategies for cartilage repair and regeneration , Stem Cell Rev. Rep. 10 (2014) 686–696.
- R.C. Lai, F. Arslan, M.M. Lee, N.S.K. Sze, A. Choo, T.S. Chen, et al., Exosome secreted by MSC reduces myocardial ischemia/reperfusion injury , Stem Cell Res. 4 (2010) 214–222.
- S. Zhang, W.C. Chu, R.C. Lai, S.K. Lim, J.H.P. Hui, W.S. Toh, Exosomes derived from human embryonic mesenchymal stem cells promote osteochondral regeneration, Osteoarthr . Cartil. 24 (2016) 2135–2140.
- S. Zhang, W. Chu, R. Lai, J. Hui, E. Lee, S. Lim, et al., 21 – human mesenchymal stem cell-derived exosomes promote orderly cartilage regeneration in an immunocompetent rat osteochondral defect model , Cytotherapy 18 (2016) S13.
- C.T. Lim, X. Ren, M.H. Afizah, S. Tarigan-Panjaitan, Z. Yang, Y. Wu, et al., Repair of osteochondral defects with rehydrated freeze-dried oligo[poly(ethylene glycol) fumarate] hydrogels seeded with bone marrow mesenchymal stem cells in a porcine model
- A. Gobbi, G. Karnatzikos, S.R. Sankineani, One-step surgery with multipotent stem cells for the treatment of large full-thickness chondral defects of the knee , Am. J. Sports Med. 42 (2014) 648–657.
- A. Gobbi, C. Scotti, G. Karnatzikos, A. Mudhigere, M. Castro, G.M. Peretti, One-step surgery with multipotent stem cells and Hyaluronan-based scaffold for the treatment of full-thickness chondral defects of the knee in patients older than 45 years , Knee Surg. Sports Traumatol. Arthrosc. (2016) 1–8.
- A. Gobbi, G. Karnatzikos, C. Scotti, V. Mahajan, L. Mazzucco, B. Grigolo, One-step cartilage repair with bone marrow aspirate concentrated cells and collagen matrix in full-thickness knee cartilage lesions: results at 2-Year follow-up , Cartilage 2 (2011) 286–299.
- K.L. Wong, K.B.L. Lee, B.C. Tai, P. Law, E.H. Lee, J.H.P. Hui, Injectable cultured bone marrow-derived mesenchymal stem cells in varus knees with cartilage defects undergoing high tibial osteotomy: a prospective, randomized controlled clinical trial with 2 years’ follow-up , Arthrosc. J. Arthrosc. Relat. Surg. 29 (2013) 2020–2028.
- J.M. Hare, J.E. Fishman, G. Gerstenblith, et al., Comparison of allogeneic vs autologous bone marrow–derived mesenchymal stem cells delivered by transendocardial injection in patients with ischemic cardiomyopathy: the poseidon randomized trial, JAMA 308 (2012) 2369–2379.
- L. Wu, J.C.H. Leijten, N. Georgi, J.N. Post, C.A. van Blitterswijk, M. Karperien, Trophic effects of mesenchymal stem cells increase chondrocyte proliferation and matrix formation , Tissue Eng. A 17 (2011) 1425–1436.
- L. Wu, H.-J. Prins, M.N. Helder, C.A. van Blitterswijk, M. Karperien, Trophic effects of mesenchymal stem cells in chondrocyte Co-Cultures are independent of culture conditions and cell sources , Tissue Eng. A 18 (2012) 1542–1551.
- S.K. Sze, D.P.V. de Kleijn, R.C. Lai, E. Khia Way Tan, H. Zhao, K.S. Yeo, et al., Elucidating the secretion proteome of human embryonic stem cell-derived mesenchymal stem cells , Mol. Cell. Proteomics 6 (2007) 1680–1689.
- M.B. Murphy, K. Moncivais, A.I. Caplan, Mesenchymal stem cells: environmentally responsive therapeutics for regenerative medicine , Exp. Mol. Med. 45 (2013) e54.
- M.J. Lee, J. Kim, M.Y. Kim, Y.-S. Bae, S.H. Ryu, T.G. Lee, et al., Proteomic analysis of tumor necrosis factor--induced secretome of human adipose tissue-derived mesenchymal stem cells , J. Proteome Res. 9 (2010) 1754–1762.
- S. Bruno, C. Grange, M.C. Deregibus, R.A. Calogero, S. Saviozzi, F. Collino, et al., Mesenchymal stem cell-derived microvesicles protect against acute tubular injury, J. Am. Soc. Nephrol. 20 (2009) 1053–1067.
- M. Yá˜nez-Mó, P.R.-M. Siljander, Z. Andreu, A.B. Zavec, F.E. Borràs, E.I. Buzas, et al. Biological properties of extracellular vesicles and their physiological functions (2015).
- C. Lawson, J.M. Vicencio, D.M. Yellon, S.M. Davidson, Microvesicles and exosomes: new players in metabolic and cardiovascular disease , J. Endocrinol. 228 (2016) R57–R71.
- A.G. Thompson, E. Gray, S.M. Heman-Ackah, I. Mager, K. Talbot, S.E. Andaloussi, et al., Extracellular vesicles in neurodegenerative diseas—pathogenesis to biomarkers, Nat. Rev. Neurol. 12 (2016) 346–357.
- I.E.M. Bank, L. Timmers, C.M. Gijsberts, Y.-N. Zhang, A. Mosterd, J.-W. Wang, et al., The diagnostic and prognostic potential of plasma extracellular vesicles for cardiovascular disease , Expert Rev. Mol. Diagn. 15 (2015) 1577–1588.
- T. Kato, S. Miyaki, H. Ishitobi, Y. Nakamura, T. Nakasa, M.K. Lotz, et al., Exosomes from IL-1 stimulated synovial fibroblasts induce osteoarthritic changes in articular chondrocytes , Arthritis. Res. Ther. 16 (2014) 1–11.
- R.W.Y. Yeo, S.K. Lim, Exosomes and their therapeutic applications, in: C. Gunther, A. Hauser, R. Huss (Eds.), Advances in Pharmaceutical Cell TherapyPrinciples of Cell-Based Biopharmaceuticals, World Scientific, Singapore, 2015, pp. 477–491.
- X. Qi, J. Zhang, H. Yuan, Z. Xu, Q. Li, X. Niu, et al., Exosomes secreted by human-Induced pluripotent stem cell-derived mesenchymal stem cells repair critical-sized bone defects through enhanced angiogenesis and osteogenesis in osteoporotic rats , Int. J. Biol. Sci. 12 (2016) 836–849.
- R.C. Lai, F. Arslan, S.S. Tan, B. Tan, A. Choo, M.M. Lee, et al., Derivation and characterization of human fetal MSCs: an alternative cell source for large-scale production of cardioprotective microparticles , J. Mol. Cell. Cardiol. 48 (2010) 1215–1224.
- Y. Zhou, H. Xu, W. Xu, B. Wang, H. Wu, Y. Tao, et al., Exosomes released by human umbilical cord mesenchymal stem cells protect against cisplatin-induced renal oxidative stress and apoptosis in vivo and in vitro , Stem Cell Res. Ther. 4 (2013) 1–13.
- Y. Qin, L. Wang, Z. Gao, G. Chen, C. Zhang, Bone marrow stromal/stem cell-derived extracellular vesicles regulate osteoblast activity and differentiation in vitro and promote bone regeneration in vivo , Sci. Rep. 6 (2016) 21961.
- M. Nakano, K. Nagaishi, N. Konari, Y. Saito, T. Chikenji, Y. Mizue, et al., Bone marrow-derived mesenchymal stem cells improve diabetes-induced cognitive impairment by exosome transfer into damaged neurons and astrocytes , Sci. Rep. 6 (2016) 24805.
- K. Nagaishi, Y. Mizue, T. Chikenji, M. Otani, M. Nakano, N. Konari, et al., Mesenchymal stem cell therapy ameliorates diabetic nephropathy via the paracrine effect of renal trophic factors including exosomes , Sci. Rep. 6 (2016) 34842.
- S.R. Baglio, K. Rooijers, D. Koppers-Lalic, F.J. Verweij, M. Pérez Lanzón, N. Zini, et al., Human bone marrow- and adipose-mesenchymal stem cells secrete exosomes enriched in distinctive miRNA and tRNA species , Stem Cell Res. Ther. 6 (2015) 1–20.
- T. Chen, R. Yeo, F. Arslan, Y. Yin, S. Tan, Efficiency of exosome production correlates inversely with the developmental maturity of MSC donor, J. Stem Cell Res. Ther. 3 (2013) 2.
- R.C. Lai, S.S. Tan, B.J. Teh, S.K. Sze, F. Arslan, D.P. de Kleijn, et al., Proteolytic potential of the MSC exosome proteome: implications for an exosome-mediated delivery of therapeutic proteasome , Int. J. Proteomics 2012 (2012) 971907.
- T.S. Chen, R.C. Lai, M.M. Lee, A.B.H. Choo, C.N. Lee, S.K. Lim, Mesenchymal stem cell secretes microparticles enriched in pre-microRNAs , Nucleic Acids Res. 38 (2010) 215–224.
- R.W. Yeo, R.C. Lai, K.H. Tan, S.K. Lim, Exosome: a novel and safer therapeutic refinement of mesenchymal stem cell, J. Circ. Biomark. 1 (2013) 7.
- R.C. Lai, R.W. Yeo, S.K. Lim, Mesenchymal stem cell exosomes, Semin. Cell Dev. Biol. 40 (2015) 82–88.
- B. Zhang, R.W. Yeo, K.H. Tan, S.K. Lim, Focus on extracellular vesicles: therapeutic potential of stem cell-derived extracellular vesicles , Int. J. Mol. Sci. 17 (2016) 174.
- Hu G-w, Q. Li, X. Niu, B. Hu, J. Liu, Zhou S-m, et al., Exosomes secreted by human-induced pluripotent stem cell-derived mesenchymal stem cells attenuate limb ischemia by promoting angiogenesis in mice , Stem Cell Res. Ther. 6 (2015) 1–15.
- J. Zhang, J. Guan, X. Niu, G. Hu, S. Guo, Q. Li, et al., Exosomes released from human induced pluripotent stem cells-derived MSCs facilitate cutaneous wound healing by promoting collagen synthesis and angiogenesis , J. Transl. Med. 13 (2015) 1–14.
- B. Zhang, M. Wang, A. Gong, X. Zhang, X. Wu, Y. Zhu, et al., HucMSC-exosome mediated-Wnt4 signaling is required for cutaneous wound healing, Stem Cells 33 (2015) 2158–2168.
- B. Zhang, Y. Yin, R.C. Lai, S.S. Tan, A.B.H. Choo, S.K. Lim, Mesenchymal stem cells secrete immunologically active exosomes , Stem Cells Dev. 23 (2013) 1233–1244.
- C.Y. Tan, R.C. Lai, W. Wong, Y.Y. Dan, S.-K. Lim, H.K. Ho, Mesenchymal stem cell-derived exosomes promote hepatic regeneration in drug-induced liver injury models , Stem Cell Res. Ther. 5 (2014) 1–14.
- C. Lee, S.A. Mitsialis, M. Aslam, S.H. Vitali, E. Vergadi, G. Konstantinou, et al., Exosomes mediate the cytoprotective action of mesenchymal stromal cells on hypoxia-induced pulmonary hypertension , Circulation 126 (2012) 2601–2611.
- B. Yu, H. Shao, C. Su, Y. Jiang, X. Chen, L. Bai, et al., Exosomes derived from MSCs ameliorate retinal laser injury partially by inhibition of MCP-1 , Sci. Rep. 6 (2016) 34562.
- Jo CH, Lee YG, Shin WH, et al. Intra-articular injection of mesenchymal stem cells for the treatment of osteoarthritis of the knee: a proof of concept clinical trial. Stem Cells. 2014;32(5):1254–66.
- Vega, Aurelio, et al. Treatment of knee osteoarthritis with allogeneic bone marrow mesenchymal stem cells: a randomized controlled trial. Transplantation. 2015;99(8):1681–90.
- Davatchi F, Sadeghi-Abdollahi B, Mohyeddin M, et al. Mesenchymal stem cell therapy for knee osteoarthritis. Preliminary report of four patients. Int J Rheum Dis. 2011;14(2):211–5
- Hernigou P, Flouzat Lachaniette CH, Delambre J, et al. Biologic augmentation of rotator cuff repair with mesenchymal stem cells during arthroscopy improves healing and prevents further tears: a case- controlled study. Int Orthop. 2014;38(9):1811–1818
- Galli D, Vitale M, Vaccarezza M. Bone marrow-derived mesenchymal cell differentiation toward myogenic lineages: facts and perspectives. Biomed Res Int. 2014;2014:6.
- Beitzel K, Solovyova O, Cote MP, et al. The future role of mesenchymal Stem cells in The management of shoulder disorders . Arthroscopy. 2013;29(10):1702–1711.
- Isaac C, Gharaibeh B, Witt M, Wright VJ, Huard J. Biologic approaches to enhance rotator cuff healing after injury. J Shoulder Elbow Surg. 2012;21(2):181–190.
- Malda, Jos, et al. " Extracellular vesicles [mdash] new tool for joint repair and regeneration. " Nature Reviews Rheumatology (2016).
Weiterführende Literatur zu PRP
- Rubio-Azpeitia E, Andia I. Partnership between platelet-rich plasma and mesenchymal stem cells: in vitro experience. Muscles Ligaments Tendons J. 2014;4(1):52–62.
Extras
- Xu, Ming, et al. " Transplanted senescent cells induce an osteoarthritis-like condition in mice. " The Journals of Gerontology Series A: Biological Sciences and Medical Sciences (2016): glw154.
- McCulloch, Kendal, Gary J. Litherland, and Taranjit Singh Rai. " Cellular senescence in osteoarthritis pathology ." Aging Cell (2017).
Patienten-Services des ANOVA Institute for Regenerative Medicine
- Das Institut liegt in Offenbach am Main, im Herzen Deutschlands, weniger als 20 Minuten vom Frankfurter Flughafen entfernt
- Individualisierte Therapie mit innovativen Stammzellprodukten
- Individuell geplante diagnostische Untersuchungen mit modernen MR- und CT-Geräten und Blutuntersuchungen
- Deutscher Qualitätsstandard (100% made in Germany) für Produktsicherheit und Qualitätssicherung
- Persönlicher Service mit freundlichen, engagierten Patientenbetreuern und Krankenschwestern
- Stetiger wissenschaftlicher Austausch mit akademischen Einrichtungen, um Ihnen die innovativsten Behandlungen im Bereich regenerative Medizin anbieten zu können