ANOVA IRM - Stammzelltherapien aus Offenbach-
Einige Erfahrungen unserer Patienten
J.R.
• Behandelt mit BMC
Arthritis der Fingergelenke
Phoebes Fortschritte:
Die rührende Geschichte einer MS-Patientin
• Behandlung mit MSEC
Erfahren Sie mehr über Phoebe, eine unserer Patientinnen mit sekundärer progressiver Multipler Sklerose. In diesem Video erklärt Sie mit eigenen Worten ihre Erfahrungen mit der ANOVA IRM. Möchten Sie mehr über Phoebe und ihren Umgang mit MS erfahren? Bitte besuchen Sie ihre Website unter www.phoebescopes.com.
Alina G. - Meniskusriss - BMC Behandlung
Alina ist selbst Arzt und war zur Behandlung ihrer Knieverletzung bei uns. Lesen Sie hier ihren selbstgeschriebenen Erfahrungsbericht (englisch).
“Fast augenblicklich wurde der entzündliche Schmerz stark gelindert. Ein paar Wochen später spürte ich bereits eine starke Steigerung der Beweglichkeit und nahm den Sport wieder nach und nach auf. Nach 6 Monaten hatte ich den Meniskusriss fast vergessen.”
Mein Name ist Alina und ich bin eine 36-jährige Ärztin im Berufsleben. Aber noch wichtiger ist mir meine Liebe zu Aktivitäten am Meer und in den Bergen.
Da Outdoor-Sportarten eine hohe Belastung und ein hohes Risiko mit sich bringen, habe ich das Glück, dass ich bis zu meinem dreißigsten Lebensjahr keine Knieverletzung hatte. Doch dann brachte ein relativ schwerer Meniskusriss meine Hobbys zum Erliegen. Jeder Hobbysportler kennt das Gefühl der Depression, wenn plötzlich nur noch die Arbeit übrig ist.
Alle orthopädischen Ärzte waren sich einig, dass eine partielle Meniskektomie (eine Operation, bei der ein Teil des Meniskus entfernt wird) die beste Option ist, um wieder gesund zu werden. Aber als Medizinerin kannte ich die möglichen Risiken und Folgen. Außerdem hat mein Mann die gleiche Operation an beiden Knien durchführen lassen. Es ist keine schnelle Genesung, die Dinge werden nicht gleich sein, und ein früh einsetzender Knorpelschaden und eine chronische Entzündung unter Belastung sind wahrscheinlich.
Ich habe von guten Ergebnissen mit PRP- und/oder Knochenmarkstammzellinjektionen gehört, aber die meisten Kliniken, die sie anbieten, waren im Ausland und wirkten nicht sehr professionell. Ich hatte das Glück, von Kollegen die Empfehlung zu erhalten, mich an Prof. Stehling und das Anova-Institut zu wenden. Dort habe ich die wahrscheinlich besten und umfangreichsten MRT-Bilder und Beratungen bekommen, die ich je bekommen habe. Prof. Stehling erläuterte mir alle aktuellen wissenschaftlichen Daten und ich traf die Entscheidung, es mit Stammzellen zu versuchen, bevor ich einen operativen Eingriff in Betracht zog.
Die Stammzellenbehandlung wurde am nächsten Tag durchgeführt und ich war mittags zu Hause. Was von da an geschah, war ziemlich bemerkenswert. Fast sofort wurden die entzündlichen Schmerzen stark gelindert. Ein paar Wochen später spürte ich schon eine große Steigerung der Beweglichkeit und ich nahm vorsichtig wieder Sport auf. Nach 6 Monaten hatte ich den Meniskusriss fast vergessen.
Alles in allem halte ich es für die beste Entscheidung, die ich je für meinen Körper und meine Zukunft als leidenschaftlicher Sportler getroffen habe, es mit einer Stammzellenbehandlung zu versuchen, bevor ich mich einer Operation unterziehe. Tausend Dank an das großartige Team von ANOVA IRM!
Alina G.
(Aus dem Englischen übersetzt)
Die folgenden Magnetresonanzbilder sind von Alina. Die obere Ebene zeigt den "Vorher"-Zustand. Eine Folge-MRT ein Jahr später zeigte etwas Bemerkenswertes. Der gerissene Meniskus war nicht nur "flach", wie es das normale ideale Ergebnis einer konservativen Therapie wäre, sondern er war auf dem MRT kaum noch zu finden. Das ist sehr erstaunlich, denn Meniskusrisse "heilen" bei Erwachsenen normalerweise nicht, nur in seltenen Fällen, wenn der Patient jung ist, der Riss nahe der Kapsel liegt und mit einer mehrwöchigen vollständigen Ruhigstellung genäht wird.
MRT
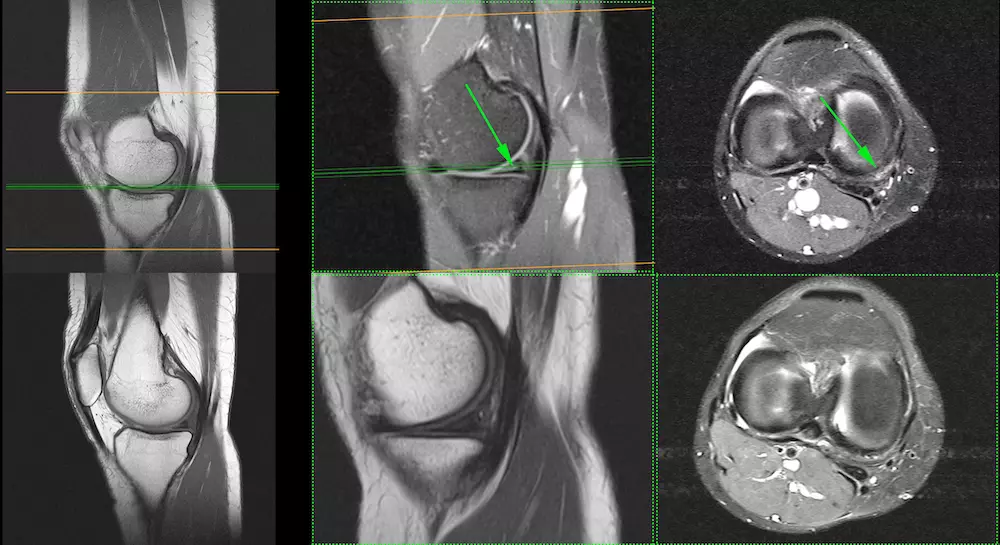
Obere Reihe: MRT vor der Behandlung, die einen Meniskusriss zeigt. Untere Reihe: MRT nach der Behandlung mittels BMC. Es wurde keine andere Behandlung durchgeführt.
E.R.G.
E.R.G. ist Hobby-Leistungssportler seit Kindesalter. Seinen ersten Bandscheibenvorfall hatte er bereits mit 25 Jahren. Lesen Sie hier seinen Erfahrungsbericht, den er selbst verfasst hat (englisch).
“Prof. Stehling entwarf einen individuellen Behandlungsplan, der die Zeit der Liposuktion einige Wochen vor der Rückenoperation festlegte. Meine erste Injektion bekam ich eine Woche nach der Operation. Die Erholung von da an war phänomenal.”
Ich bin seit meiner Kindheit sportbegeistert. Ich habe aktiv Gymnastik, Langstreckenlauf, Wintersport und Sportklettern auf Wettkampfniveau betrieben. Das hat meinem Körper einiges abverlangt. Meinen ersten Bandscheibenvorfall hatte ich mit 25 Jahren diagnostiziert.
Weitere 7 Jahre lang behandelte ich diesen Bandscheibenvorfall mit konservativer Therapie, d. h. mit täglicher rückengerechter Gymnastik und gelegentlicher Einnahme von Schmerzmitteln, aber vor allem mit Zurückhaltung bei rückenintensiven Sportarten, in meinem Fall Laufen und Turnen.
Trotzdem verschlimmerte sich der Zustand. Irgendwann konnte ich ein Bein nicht mehr bewegen und war auf morphiumhaltige Schmerzmittel angewiesen, um zur Arbeit gehen zu können.
Eine Operation war unausweichlich. Aber ich hatte gehört, dass die Operation zwar eine sofortige Schmerzlinderung bringt, dass diese Ergebnisse aber oft nicht von Dauer sind. Ich hatte Angst, dass es auf lange Sicht nicht besser werden würde. Der Gedanke, wieder in diesen Zustand zu geraten und sogar das Klettern aufgeben zu müssen, versetzte mich in Panik. Ich wollte alles Mögliche versuchen, um meine Chancen zu maximieren, wieder in einen körperlich einwandfreien Zustand zu gelangen.
Ich las Forschungsergebnisse über Stammzelltherapien bei degenerativen Erkrankungen. Ich wusste sofort, dass ich meine Genesung mit einer kontinuierlichen Stammzellenbehandlung verbinden wollte. Die mit Abstand fortschrittlichste und wissenschaftlich fundierteste Antwort erhielt ich vom Team des Anova-Instituts für Regenerative Medizin, genauer gesagt von Prof. Stehling.
Der Ansatz, die parakrinen Faktoren (Stammzellsekretome, Exosomen) aus Ihren Stammzellen in einer Laborumgebung zu extrahieren, ist viel sinnvoller als eine einzelne Injektion mit Knochenmarkskonzentrat oder sogar potenziell gefährliche Ansätze, bei denen MSCs in einem nicht überprüften Verfahren in Ländern wie Thailand, Russland oder China gezüchtet werden.
Prof. Stehling entwarf ein individuelles Konzept, bei dem der Zeitpunkt der Fettabsaugung einige Wochen vor der Rückenoperation angesetzt wurde. Meine erste Injektion erhielt ich eine Woche nach der Operation. Die Genesung von da an war phänomenal. Einige Tage später konnte ich wieder arbeiten, ein paar Wochen später konnte ich wieder alles tun, was ich liebe, und hatte seitdem keine Probleme mehr. Mehr noch: Sogar meine Knie und Knöchel, die mich nie wirklich gestört haben, aber irgendwie chronisch juckten, fühlen sich wieder an wie in meinen Zwanzigern. Sogar eine zehn Jahre alte Verletzung, die mir eine versteifte Fingerkapsel bescherte, ist vollständig verheilt - was gelinde gesagt erstaunlich ist.
Zusätzlich zur Therapie gab mir der Arzt einige gute Ratschläge, die auf aktuellen Forschungsergebnissen beruhen, wie gelegentliche Fastenkuren und die Entschlackung seneszenter Zellen mit leicht verfügbaren Substanzen. Ich bin mir bewusst, dass das Altern weitergehen wird, aber momentan fühlt es sich nicht so an :-)
Es ist zwar nicht medizinisch relevant, aber ich genieße die jährlichen Besuche beim Anova-Team sehr: Das Team ist super nett und lustig, und meistens trifft man dort auch einen Prominenten.
Auf jeden Fall bin ich dem großartigen Team von Anova für immer dankbar für ihre unglaubliche Stammzelltherapie und den individuellen Behandlungsplan, den sie für mich erstellt haben und der mein Leben so viel besser gemacht hat!
E.R.G.
(Aus dem Englischen übersetzt)
Ryan Donovan - Erektile Dysfunktion - BMC Behandlung
"Ich bin ein 30 Jahre alter Mann. Ich habe immer Sport getrieben, um meinen Körper gesund zu halten, und ich ernähre mich ausgewogen. Leider erlitt ich vor drei Jahren ein lokales Trauma, das bei mir zu einer gewissen erektilen Dysfunktion führte. Nachdem ich konventionelle Therapien ausprobiert hatte, wandte ich mich an ANOVA, um zu versuchen, einen kurativen - und nicht nur palliativen - Ansatz für meinen Zustand zu finden. Ich muss Herrn Martinovic und dem gesamten ANOVA-Team danken, die meinen Fall vom ersten Kontakt an mit Diskretion und Würde behandelt haben. Frau Dr. Sabow, bei der ich das ärztliche Gespräch und später den Eingriff hatte, war außerordentlich kompetent und professionell. Sie gab mir eine realistische Beschreibung der Ergebnisse, die ich von der von mir gewählten Therapie (BMC für erektile Dysfunktion) zu erwarten hatte. Die Klinik ist modern, und das gesamte Team ist sehr kompetent. Der Eingriff verlief reibungslos, und 3 Monate später kann ich mich über messbare Verbesserungen meines Zustands und meiner Lebensqualität freuen."
Ryan Donovan ( Aus dem Englischen übersetzt )
Weiterführende Literatur zu MSC, BMC, Stamzellen Secretom und EVs
- Georg Hansmann, Philippe Chouvarine, Franziska Diekmann, Martin Giera, Markus Ralser, Michael Mülleder, Constantin von Kaisenberg, Harald Bertram, Ekaterina Legchenko & Ralf Hass "Human umbilical cord mesenchymal stem cell-derived treatment of severe pulmonary arterial hypertension". Nature Cardiovascular Research volume 1, pages568–576 (2022).
- Murphy JM, Fink DJ, Hunziker EB, et al. Stem cell therapy in a caprine model of osteoarthritis . Arthritis Rheum. 2003;48:3464–74.
- Lee KB, Hui JH, Song IC, Ardany L, et al. Injectable mesenchymal stem cell therapy for large cartilage defects—a porcine model. Stem Cell. 2007;25:2964–71.
- Saw KY, Hussin P, Loke SC, et al. Articular cartilage regeneration with autologous marrow aspirate and hyaluronic acid: an experimental study in a goat model. Arthroscopy . 2009;25(12):1391–400.
- Black L, Gaynor J, Adams C, et al. Effect of intra-articular injection of autologous adipose-derived mesenchymal stem and regenerative cells on clinical signs of chronic osteoarthritis of the elbow joint in dogs. Vet Ther. 2008;9:192-200.
- Centeno C, Busse D, Kisiday J, et al. Increased knee cartilage volume in degenerative joint disease using percutaneously implanted, autologous mesenchymal stem cells. Pain Physician. 2008;11(3):343–53.
- Centeno C, Kisiday J, Freeman M, et al. Partial regeneration of the human hip via autologous bone marrow nucleated cell transfer: a case study. Pain Physician. 2006;9:253–6.
- Centeno C, Schultz J, Cheever M. Safety and complications reporting on the re-implantation of culture-expanded mesenchymal stem cells using autologous platelet lysate technique. Curr Stem Cell. 2011;5(1):81–93.
- Pak J. Regeneration of human bones in hip osteonecrosis and human cartilage in knee osteoarthritis with autologous adipose derived stem cells: a case series. J Med Case Rep. 2001;5:296.
- Kuroda R, Ishida K, et al. Treatment of a full-thickness articular cartilage defect in the femoral condyle of an athlete with autologous bone-marrow stromal cells. Osteoarthritis Cartilage. 2007;15:226–31.
- Emadedin M, Aghdami N, Taghiyar L, et al. Intra-articular injection of autologous mesenchymal stem cells in six patients with knee osteoarthritis. Arch Iran Med. 2012;15(7):422–8.
- Saw KY et al. Articular cartilage regeneration with autologous peripheral blood stem cells versus hyaluronic acid: a randomized controlled trial. Arthroscopy. 2013;29(4):684–94.
- Vangsness CT, Farr J, Boyd J, et al. Adult human mesenchymal stem cells delivered via intra-articular injection to the knee following partial medial meniscectomy. J Bone Joint Surg. 2014;96(2):90–8.
- Freitag, Julien, et al. Mesenchymal stem cell therapy in the treatment of osteoarthritis: reparative pathways, safety and efficacy–a review. BMC musculoskeletal disorders 17.1 (2016): 230.
- Maumus, Marie, Christian Jorgensen, and Danièle Noël. " Mesenchymal stem cells in regenerative medicine applied to rheumatic diseases: role of secretome and exosomes. " Biochimie 95.12 (2013): 2229-2234.
- Dostert, Gabriel, et al. " How do mesenchymal stem cells influence or are influenced by microenvironment through extracellular vesicles communication?. " Frontiers in Cell and Developmental Biology 5 (2017).
- Chaparro, Orlando, and Itali Linero. " Regenerative Medicine: A New Paradigm in Bone Regeneration. " (2016).
- Toh, Wei Seong, et al. " MSC exosome as a cell-free MSC therapy for cartilage regeneration: Implications for osteoarthritis treatment. " Seminars in Cell & Developmental Biology. Academic Press, 2016.
- Chaparro, Orlando, and Itali Linero. " Regenerative Medicine: A New Paradigm in Bone Regeneration. " (2016).
- S. Koelling, J. Kruegel, M. Irmer, J.R. Path, B. Sadowski, X. Miro, et al., Migratory chondrogenic progenitor cells from repair tissue during the later stages of human osteoarthritis , Cell Stem Cell 4 (2009) 324–335.
- B.A. Jones, M. Pei, Synovium-Derived stem cells: a tissue-Specific stem cell for cartilage engineering and regeneration , Tissue Eng. B: Rev. 18 (2012) 301–311.
- W. Ando, J.J. Kutcher, R. Krawetz, A. Sen, N. Nakamura, C.B. Frank, et al., Clonal analysis of synovial fluid stem cells to characterize and identify stable mesenchymal stromal cell/mesenchymal progenitor cell phenotypes in a porcine model: a cell source with enhanced commitment to the chondrogenic lineage, Cytotherapy 16 (2014) 776–788.
- K.B.L. Lee, J.H.P. Hui, I.C. Song, L. Ardany, E.H. Lee, Injectable mesenchymal stem cell therapy for large cartilage defects—a porcine model, Stem Cells 25 (2007) 2964–2971.
- W.-L. Fu, C.-Y. Zhou, J.-K. Yu, A new source of mesenchymal stem cells for articular cartilage repair: mSCs derived from mobilized peripheral blood share similar biological characteristics in vitro and chondrogenesis in vivo as MSCs from bone marrow in a rabbit model , Am. J. Sports Med. 42 (2014) 592–601.
- X. Xie, Y. Wang, C. Zhao, S. Guo, S. Liu, W. Jia, et al., Comparative evaluation of MSCs from bone marrow and adipose tissue seeded in PRP-derived scaffold for cartilage regeneration , Biomaterials 33 (2012) 7008–7018.
- E.-R. Chiang, H.-L. Ma, J.-P. Wang, C.-L. Liu, T.-H. Chen, S.-C. Hung, Allogeneic mesenchymal stem cells in combination with hyaluronic acid for the treatment of osteoarthritis in rabbits , PLoS One 11 (2016) e0149835.
- H. Nejadnik, J.H. Hui, E.P. Feng Choong, B.-C. Tai, E.H. Lee, Autologous bone marrow–derived mesenchymal stem cells versus autologous chondrocyte implantation: an observational cohort study , Am. J. Sports Med. 38 (2010) 1110–1116.
- I. Sekiya, T. Muneta, M. Horie, H. Koga, Arthroscopic transplantation of synovial stem cells improves clinical outcomes in knees with cartilage defects , Clin. Orthop. Rel. Res. 473 (2015) 2316–2326.
- Y.S. Kim, Y.J. Choi, Y.G. Koh, Mesenchymal stem cell implantation in knee osteoarthritis: an assessment of the factors influencing clinical outcomes , Am. J. Sports Med. 43 (2015) 2293–2301.
- W.-L. Fu, Y.-F. Ao, X.-Y. Ke, Z.-Z. Zheng, X. Gong, D. Jiang, et al., Repair of large full-thickness cartilage defect by activating endogenous peripheral blood stem cells and autologous periosteum flap transplantation combined with patellofemoral realignment , Knee 21 (2014) 609–612.
- Y.-G. Koh, O.-R. Kwon, Y.-S. Kim, Y.-J. Choi, D.-H. Tak, Adipose-derived mesenchymal stem cells with microfracture versus microfracture alone: 2-year follow-up of a prospective randomized trial , Arthrosc. J. Arthrosc. Relat. Surg. 32 (2016) 97–109.
- T.S. de Windt, L.A. Vonk, I.C.M. Slaper-Cortenbach, M.P.H. van den Broek, R. Nizak, M.H.P. van Rijen, et al., Allogeneic mesenchymal stem cells stimulate cartilage regeneration and are safe for single-Stage cartilage repair in humans upon mixture with recycled autologous chondrons , Stem Cells (2016) (n/a-n/a).
- L. da Silva Meirelles, A.M. Fontes, D.T. Covas, A.I. Caplan, Mechanisms involved in the therapeutic properties of mesenchymal stem cells , Cytokine Growth Factor Rev. 20 (2009) 419–427.
- W.S. Toh, C.B. Foldager, M. Pei, J.H.P. Hui, Advances in mesenchymal stem cell-based strategies for cartilage repair and regeneration , Stem Cell Rev. Rep. 10 (2014) 686–696.
- R.C. Lai, F. Arslan, M.M. Lee, N.S.K. Sze, A. Choo, T.S. Chen, et al., Exosome secreted by MSC reduces myocardial ischemia/reperfusion injury , Stem Cell Res. 4 (2010) 214–222.
- S. Zhang, W.C. Chu, R.C. Lai, S.K. Lim, J.H.P. Hui, W.S. Toh, Exosomes derived from human embryonic mesenchymal stem cells promote osteochondral regeneration, Osteoarthr . Cartil. 24 (2016) 2135–2140.
- S. Zhang, W. Chu, R. Lai, J. Hui, E. Lee, S. Lim, et al., 21 – human mesenchymal stem cell-derived exosomes promote orderly cartilage regeneration in an immunocompetent rat osteochondral defect model , Cytotherapy 18 (2016) S13.
- C.T. Lim, X. Ren, M.H. Afizah, S. Tarigan-Panjaitan, Z. Yang, Y. Wu, et al., Repair of osteochondral defects with rehydrated freeze-dried oligo[poly(ethylene glycol) fumarate] hydrogels seeded with bone marrow mesenchymal stem cells in a porcine model
- A. Gobbi, G. Karnatzikos, S.R. Sankineani, One-step surgery with multipotent stem cells for the treatment of large full-thickness chondral defects of the knee , Am. J. Sports Med. 42 (2014) 648–657.
- A. Gobbi, C. Scotti, G. Karnatzikos, A. Mudhigere, M. Castro, G.M. Peretti, One-step surgery with multipotent stem cells and Hyaluronan-based scaffold for the treatment of full-thickness chondral defects of the knee in patients older than 45 years , Knee Surg. Sports Traumatol. Arthrosc. (2016) 1–8.
- A. Gobbi, G. Karnatzikos, C. Scotti, V. Mahajan, L. Mazzucco, B. Grigolo, One-step cartilage repair with bone marrow aspirate concentrated cells and collagen matrix in full-thickness knee cartilage lesions: results at 2-Year follow-up , Cartilage 2 (2011) 286–299.
- K.L. Wong, K.B.L. Lee, B.C. Tai, P. Law, E.H. Lee, J.H.P. Hui, Injectable cultured bone marrow-derived mesenchymal stem cells in varus knees with cartilage defects undergoing high tibial osteotomy: a prospective, randomized controlled clinical trial with 2 years’ follow-up , Arthrosc. J. Arthrosc. Relat. Surg. 29 (2013) 2020–2028.
- J.M. Hare, J.E. Fishman, G. Gerstenblith, et al., Comparison of allogeneic vs autologous bone marrow–derived mesenchymal stem cells delivered by transendocardial injection in patients with ischemic cardiomyopathy: the poseidon randomized trial, JAMA 308 (2012) 2369–2379.
- L. Wu, J.C.H. Leijten, N. Georgi, J.N. Post, C.A. van Blitterswijk, M. Karperien, Trophic effects of mesenchymal stem cells increase chondrocyte proliferation and matrix formation , Tissue Eng. A 17 (2011) 1425–1436.
- L. Wu, H.-J. Prins, M.N. Helder, C.A. van Blitterswijk, M. Karperien, Trophic effects of mesenchymal stem cells in chondrocyte Co-Cultures are independent of culture conditions and cell sources , Tissue Eng. A 18 (2012) 1542–1551.
- S.K. Sze, D.P.V. de Kleijn, R.C. Lai, E. Khia Way Tan, H. Zhao, K.S. Yeo, et al., Elucidating the secretion proteome of human embryonic stem cell-derived mesenchymal stem cells , Mol. Cell. Proteomics 6 (2007) 1680–1689.
- M.B. Murphy, K. Moncivais, A.I. Caplan, Mesenchymal stem cells: environmentally responsive therapeutics for regenerative medicine , Exp. Mol. Med. 45 (2013) e54.
- M.J. Lee, J. Kim, M.Y. Kim, Y.-S. Bae, S.H. Ryu, T.G. Lee, et al., Proteomic analysis of tumor necrosis factor--induced secretome of human adipose tissue-derived mesenchymal stem cells , J. Proteome Res. 9 (2010) 1754–1762.
- S. Bruno, C. Grange, M.C. Deregibus, R.A. Calogero, S. Saviozzi, F. Collino, et al., Mesenchymal stem cell-derived microvesicles protect against acute tubular injury, J. Am. Soc. Nephrol. 20 (2009) 1053–1067.
- M. Yá˜nez-Mó, P.R.-M. Siljander, Z. Andreu, A.B. Zavec, F.E. Borràs, E.I. Buzas, et al. Biological properties of extracellular vesicles and their physiological functions (2015).
- C. Lawson, J.M. Vicencio, D.M. Yellon, S.M. Davidson, Microvesicles and exosomes: new players in metabolic and cardiovascular disease , J. Endocrinol. 228 (2016) R57–R71.
- A.G. Thompson, E. Gray, S.M. Heman-Ackah, I. Mager, K. Talbot, S.E. Andaloussi, et al., Extracellular vesicles in neurodegenerative diseas—pathogenesis to biomarkers, Nat. Rev. Neurol. 12 (2016) 346–357.
- I.E.M. Bank, L. Timmers, C.M. Gijsberts, Y.-N. Zhang, A. Mosterd, J.-W. Wang, et al., The diagnostic and prognostic potential of plasma extracellular vesicles for cardiovascular disease , Expert Rev. Mol. Diagn. 15 (2015) 1577–1588.
- T. Kato, S. Miyaki, H. Ishitobi, Y. Nakamura, T. Nakasa, M.K. Lotz, et al., Exosomes from IL-1 stimulated synovial fibroblasts induce osteoarthritic changes in articular chondrocytes , Arthritis. Res. Ther. 16 (2014) 1–11.
- R.W.Y. Yeo, S.K. Lim, Exosomes and their therapeutic applications, in: C. Gunther, A. Hauser, R. Huss (Eds.), Advances in Pharmaceutical Cell TherapyPrinciples of Cell-Based Biopharmaceuticals, World Scientific, Singapore, 2015, pp. 477–491.
- X. Qi, J. Zhang, H. Yuan, Z. Xu, Q. Li, X. Niu, et al., Exosomes secreted by human-Induced pluripotent stem cell-derived mesenchymal stem cells repair critical-sized bone defects through enhanced angiogenesis and osteogenesis in osteoporotic rats , Int. J. Biol. Sci. 12 (2016) 836–849.
- R.C. Lai, F. Arslan, S.S. Tan, B. Tan, A. Choo, M.M. Lee, et al., Derivation and characterization of human fetal MSCs: an alternative cell source for large-scale production of cardioprotective microparticles , J. Mol. Cell. Cardiol. 48 (2010) 1215–1224.
- Y. Zhou, H. Xu, W. Xu, B. Wang, H. Wu, Y. Tao, et al., Exosomes released by human umbilical cord mesenchymal stem cells protect against cisplatin-induced renal oxidative stress and apoptosis in vivo and in vitro , Stem Cell Res. Ther. 4 (2013) 1–13.
- Y. Qin, L. Wang, Z. Gao, G. Chen, C. Zhang, Bone marrow stromal/stem cell-derived extracellular vesicles regulate osteoblast activity and differentiation in vitro and promote bone regeneration in vivo , Sci. Rep. 6 (2016) 21961.
- M. Nakano, K. Nagaishi, N. Konari, Y. Saito, T. Chikenji, Y. Mizue, et al., Bone marrow-derived mesenchymal stem cells improve diabetes-induced cognitive impairment by exosome transfer into damaged neurons and astrocytes , Sci. Rep. 6 (2016) 24805.
- K. Nagaishi, Y. Mizue, T. Chikenji, M. Otani, M. Nakano, N. Konari, et al., Mesenchymal stem cell therapy ameliorates diabetic nephropathy via the paracrine effect of renal trophic factors including exosomes , Sci. Rep. 6 (2016) 34842.
- S.R. Baglio, K. Rooijers, D. Koppers-Lalic, F.J. Verweij, M. Pérez Lanzón, N. Zini, et al., Human bone marrow- and adipose-mesenchymal stem cells secrete exosomes enriched in distinctive miRNA and tRNA species , Stem Cell Res. Ther. 6 (2015) 1–20.
- T. Chen, R. Yeo, F. Arslan, Y. Yin, S. Tan, Efficiency of exosome production correlates inversely with the developmental maturity of MSC donor, J. Stem Cell Res. Ther. 3 (2013) 2.
- R.C. Lai, S.S. Tan, B.J. Teh, S.K. Sze, F. Arslan, D.P. de Kleijn, et al., Proteolytic potential of the MSC exosome proteome: implications for an exosome-mediated delivery of therapeutic proteasome , Int. J. Proteomics 2012 (2012) 971907.
- T.S. Chen, R.C. Lai, M.M. Lee, A.B.H. Choo, C.N. Lee, S.K. Lim, Mesenchymal stem cell secretes microparticles enriched in pre-microRNAs , Nucleic Acids Res. 38 (2010) 215–224.
- R.W. Yeo, R.C. Lai, K.H. Tan, S.K. Lim, Exosome: a novel and safer therapeutic refinement of mesenchymal stem cell, J. Circ. Biomark. 1 (2013) 7.
- R.C. Lai, R.W. Yeo, S.K. Lim, Mesenchymal stem cell exosomes, Semin. Cell Dev. Biol. 40 (2015) 82–88.
- B. Zhang, R.W. Yeo, K.H. Tan, S.K. Lim, Focus on extracellular vesicles: therapeutic potential of stem cell-derived extracellular vesicles , Int. J. Mol. Sci. 17 (2016) 174.
- Hu G-w, Q. Li, X. Niu, B. Hu, J. Liu, Zhou S-m, et al., Exosomes secreted by human-induced pluripotent stem cell-derived mesenchymal stem cells attenuate limb ischemia by promoting angiogenesis in mice , Stem Cell Res. Ther. 6 (2015) 1–15.
- J. Zhang, J. Guan, X. Niu, G. Hu, S. Guo, Q. Li, et al., Exosomes released from human induced pluripotent stem cells-derived MSCs facilitate cutaneous wound healing by promoting collagen synthesis and angiogenesis , J. Transl. Med. 13 (2015) 1–14.
- B. Zhang, M. Wang, A. Gong, X. Zhang, X. Wu, Y. Zhu, et al., HucMSC-exosome mediated-Wnt4 signaling is required for cutaneous wound healing, Stem Cells 33 (2015) 2158–2168.
- B. Zhang, Y. Yin, R.C. Lai, S.S. Tan, A.B.H. Choo, S.K. Lim, Mesenchymal stem cells secrete immunologically active exosomes , Stem Cells Dev. 23 (2013) 1233–1244.
- C.Y. Tan, R.C. Lai, W. Wong, Y.Y. Dan, S.-K. Lim, H.K. Ho, Mesenchymal stem cell-derived exosomes promote hepatic regeneration in drug-induced liver injury models , Stem Cell Res. Ther. 5 (2014) 1–14.
- C. Lee, S.A. Mitsialis, M. Aslam, S.H. Vitali, E. Vergadi, G. Konstantinou, et al., Exosomes mediate the cytoprotective action of mesenchymal stromal cells on hypoxia-induced pulmonary hypertension , Circulation 126 (2012) 2601–2611.
- B. Yu, H. Shao, C. Su, Y. Jiang, X. Chen, L. Bai, et al., Exosomes derived from MSCs ameliorate retinal laser injury partially by inhibition of MCP-1 , Sci. Rep. 6 (2016) 34562.
- Jo CH, Lee YG, Shin WH, et al. Intra-articular injection of mesenchymal stem cells for the treatment of osteoarthritis of the knee: a proof of concept clinical trial. Stem Cells. 2014;32(5):1254–66.
- Vega, Aurelio, et al. Treatment of knee osteoarthritis with allogeneic bone marrow mesenchymal stem cells: a randomized controlled trial. Transplantation. 2015;99(8):1681–90.
- Davatchi F, Sadeghi-Abdollahi B, Mohyeddin M, et al. Mesenchymal stem cell therapy for knee osteoarthritis. Preliminary report of four patients. Int J Rheum Dis. 2011;14(2):211–5
- Hernigou P, Flouzat Lachaniette CH, Delambre J, et al. Biologic augmentation of rotator cuff repair with mesenchymal stem cells during arthroscopy improves healing and prevents further tears: a case- controlled study. Int Orthop. 2014;38(9):1811–1818
- Galli D, Vitale M, Vaccarezza M. Bone marrow-derived mesenchymal cell differentiation toward myogenic lineages: facts and perspectives. Biomed Res Int. 2014;2014:6.
- Beitzel K, Solovyova O, Cote MP, et al. The future role of mesenchymal Stem cells in The management of shoulder disorders . Arthroscopy. 2013;29(10):1702–1711.
- Isaac C, Gharaibeh B, Witt M, Wright VJ, Huard J. Biologic approaches to enhance rotator cuff healing after injury. J Shoulder Elbow Surg. 2012;21(2):181–190.
- Malda, Jos, et al. " Extracellular vesicles [mdash] new tool for joint repair and regeneration. " Nature Reviews Rheumatology (2016).
Weiterführende Literatur zu PRP
- Rubio-Azpeitia E, Andia I. Partnership between platelet-rich plasma and mesenchymal stem cells: in vitro experience. Muscles Ligaments Tendons J. 2014;4(1):52–62.
Extras
- Xu, Ming, et al. " Transplanted senescent cells induce an osteoarthritis-like condition in mice. " The Journals of Gerontology Series A: Biological Sciences and Medical Sciences (2016): glw154.
- McCulloch, Kendal, Gary J. Litherland, and Taranjit Singh Rai. " Cellular senescence in osteoarthritis pathology ." Aging Cell (2017).
Patienten-Services des ANOVA Institute for Regenerative Medicine
- Das Institut liegt in Offenbach am Main, im Herzen Deutschlands, weniger als 20 Minuten vom Frankfurter Flughafen entfernt
- Individualisierte Therapie mit innovativen Stammzellprodukten
- Individuell geplante diagnostische Untersuchungen mit modernen MR- und CT-Geräten und Blutuntersuchungen
- Deutscher Qualitätsstandard (100% made in Germany) für Produktsicherheit und Qualitätssicherung
- Persönlicher Service mit freundlichen, engagierten Patientenbetreuern und Krankenschwestern
- Stetiger wissenschaftlicher Austausch mit akademischen Einrichtungen, um Ihnen die innovativsten Behandlungen im Bereich regenerative Medizin anbieten zu können
